Mücken, die gegen Malaria immun gemacht werden, könnten helfen, die Krankheit auszurotten

[ad_1]

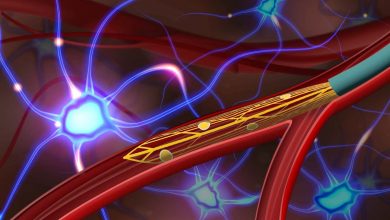
Eine weibliche Anopheles gambiae-Mücke. Seine roten Augen weisen auf das Vorhandensein eines veränderten Gens hin, das Malariaresistenz verleihen soll
Rebeca Carballar-Lejarazú
Mücken wurden gentechnisch verändert, sodass sie gegen die Parasiten, die Malaria verursachen, immun sind.
Wenn die genetische Veränderung in die Wildnis freigesetzt wird, sollte sie sich in einer Mückenpopulation ausbreiten, da sie eine Sequenz enthält, die als „Gene Drive“ bekannt ist. Dies bedeutet, dass alle Nachkommen der veränderten Insekten die Immunität erben würden. Dieser Ansatz könnte die Zahl der Malariafälle bei Menschen senken.
Malaria ist eine der weltweit häufigsten Todes- und Krankheitsursachen und fordert insbesondere bei kleinen Kindern in Afrika südlich der Sahara einen hohen Tribut. Kürzlich wurden zwei Impfstoffe entwickelt, die jedoch nur eine teilweise Immunität verleihen.
Weitere High-Tech-Strategien gegen durch Mücken übertragene Krankheiten werden derzeit untersucht, darunter Gene Drives, die alle Mücken in einem Zielgebiet töten. Diese könnten jedoch unvorhersehbare Auswirkungen auf Ökosysteme haben, heißt es Anthony James an der University of California, Irvine.
Der Ansatz seines Teams lässt Mücken leben, sorgt aber dafür, dass sie Antikörper produzieren, die den wichtigsten Malaria-verursachenden Parasiten, einen sogenannten einzelligen Organismus, abtöten Plasmodium falciparum.
Die eingefügte DNA umfasst die Gene für zwei Antikörperfragmente; Jeder von ihnen zielt auf den Parasiten in einem anderen Stadium seines Lebenszyklus bei Mücken ab. Dies verringert die Wahrscheinlichkeit, dass der Parasit eine Resistenz entwickelt, sagt James.
Es trägt auch eine Sequenz, die bedeutet, dass es sich in der Bevölkerung verbreiten sollte. Es soll sich in ein Gen einfügen für die Augenfarbe, was bedeutet, dass alle modifizierten Mücken rote Augen haben, was bei der Überwachung des Erfolgs der Strategie hilft.
Die DNA kodiert für ein Enzym namens Cas9 – das auch in CRISPR-basierten Genbearbeitungstherapien verwendet wird – sowie für eine „Leit“-DNA-Sequenz, die bedeutet, dass das Enzym nur auf das Augenpigment-Gen abzielt.
Die Nachkommen einer veränderten Mücke und einer normalen Mücke haben zunächst ein verändertes und ein normales Augenpigment-Gen. Aber das Cas9-Enzym macht einen Bruch im normalen Gen, dann nutzen die üblichen DNA-Reparaturenzyme die manipulierte DNA als Vorlage und kopieren diese Sequenz in das normale Gen – so haben die Nachkommen als Ergebnis zwei veränderte Gene.
Bei Tests im Labor erwies sich das System bei einer Mückenart, der sogenannten Mückenart, als unwirksam Anopheles Gambiae, weil die Männchen dadurch weniger erfolgreich bei der Paarung waren. Dieser Nachteil wurde jedoch bei einer anderen Mückenart namens Mücke nicht beobachtet Anopheles coluzzii.
Bei dieser Art verbreitete sich das Gen schnell durch kleine Mückenkäfige und sie beherbergten daher weniger Parasiten als unveränderte Insekten. Auf dieser Grundlage errechnete das Team, dass die Malariafälle beim Menschen innerhalb von drei Monaten um mehr als 90 Prozent reduziert werden könnten, wenn modifizierte Mücken unter optimalen Bedingungen auf einer Insel freigesetzt würden.
Die Forscher führen derzeit Gespräche, um den Ansatz auf der Insel São Tomé vor der Westküste Afrikas zu testen A. coluzii Mücken sind eine der Hauptursachen für Malaria.
„Sie haben einen ziemlich guten Anti-Pathogen-Effektor und einen ziemlich guten Gene Drive in einem einzigen Paket zusammengestellt“, sagt er Luke Alphey an der University of York, Großbritannien. Alphey war Mitbegründer einer Firma namens Oxitec Dabei kommt eine andere Technik zum Einsatz, bei der mit Bakterien infizierte Mücken freigesetzt werden Wolbachiadas den Dengue-Virus nicht verbreiten kann.
Sadie Ryan an der University of Florida in Gainesville sagt, dass Methoden zur Malariabekämpfung, die die Insekten nicht ausrotten, aus ökologischer Sicht besser sein könnten, da die Mücken immer noch eine Rolle im Ökosystem spielen können.
Themen:
[ad_2]
Source link